Cari Lettori,
è balzato agli onori della cronaca di diverse testate medico-scientifiche divulgative, inclusa questa, la notizia che un gruppo di gastroenterologi di Tokyo avrebbe sperimentato – su topi e maiali – una nuova tecnica per somministrare ossigeno a soggetti con problemi respiratori per una strada “poco convenzionale”: il retto. (https://www.sanitainsicilia.it/innovazione-scientifica-nuovi-metodi-di-ventilazione-col-retto_409879/).
In particolare, i ricercatori hanno anestetizzato alcune cavie in un ambiente con bassa concentrazione di
ossigeno e hanno quindi sperimentato un innovativo metodo per introdurre ossigeno nel retto di questi
animali. La procedura determinava un allungamento della sopravvivenza delle cavie, alle quali si era anche provveduto ad effettuare un raschiamento della parete di quel tratto di intestino, una pratica dagli stessi autori definita “invasiva e difficile da riprodurre negli esseri umani”.
Allora perché quest’attenzione mediatica? Potrebbe realmente una pratica di questo genere essere traslata nell’uomo, con successo? Molte sono le perplessità che una buona conoscenza dell’anatomia delle regioni oggetto d’interesse suscita. Ve ne esporrò alcune.
Innanzitutto, trovo utile partire da un breve inquadramento anatomico del retto. L’apparato digerente si suddivide nel canale alimentare e negli organi annessi (denti, lingua, ghiandole salivari maggiori, fegato, pancreas, appendice vermiforme). Il canale alimentare è un lungo condotto che si origina nella cavità orale e si continua con faringe, esofago, stomaco, intestino e canale anale. L’intestino è il tratto più lungo, suddividendosi in “intestino tenue” (l’insieme di duodeno, digiuno e ileo) e “intestino crasso“ (costituito da cieco, colon e, per l’appunto, retto).
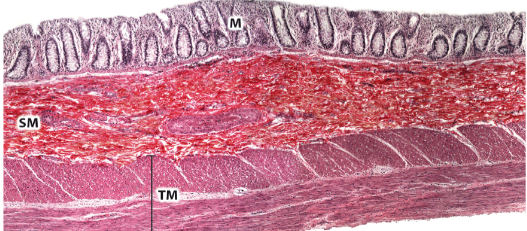
Il canale alimentare si caratterizza per un rivestimento interno costituito da un insieme di tessuti che,
collettivamente, prendono il nome di “tonaca mucosa”. Questa è costituita a sua volta da tre strati
sovrapposti: l’epitelio di rivestimento, la lamina propria e la muscolaris mucosae (letteralmente, dal latino, “la tonaca muscolare della tonaca mucosa”).

Professore Francesco Cappello
Senza perderci in troppi dettagli, non utili per il ragionamento che stiamo portando avanti, l’epitelio della mucosa della metà sovradiaframmatica del canale alimentare è un epitelio spesso (pluristratificato) in quanto deve conferire alla mucosa resistenza ai traumi meccanici derivanti dalla masticazione e dal trasporto del cibo – attraverso la deglutizione – nello stomaco. Quest’ultimo organo e l’intestino, invece, sono caratterizzati da un epitelio di tipo semplice, con un unico strato di cellule alte (“colonnari”) preposte allo svolgimento di funzioni di secrezione e assorbimento.
Ad esempio, le cellule dell’epitelio gastrico secernono – tra le altre cose – alcuni enzimi digestivi (tra cui il pepsinogeno), l’acido cloridrico (che attiva il pepsinogeno, convertendolo in pepsina, fondamentale per la digestione delle proteine) e il muco (che forma un film protettivo per impedire che l’acido lesioni la parete gastrica determinandone una sorta di “autodigestione”). Viceversa, le cellule epiteliali dell’intestino sono per lo più funzionali all’assorbimento dei nutrienti digeriti, nonché dell’acqua e dei sali minerali. Le cellule epiteliali del retto invece si caratterizzano funzionalmente per la produzione del muco necessario a lubrificarne la superficie interna e consentire un fluido scorrimento del materiale fecale durante l’evacuazione.
L’epitelio, come detto, poggia su una lamina propria, un sottile strato di tessuto connettivo che contiene – tra l’altro – i vasi ematici funzionali ad apportare ossigeno e altre sostanze metaboliche all’epitelio, che per ovvie ragioni funzionali è privo di vasi (avascolare), in quanto la loro presenza determinerebbe un continuo sanguinamento ad ogni minimo traumatismo. Tuttavia, i vasi della lamina propria sono davvero modesti, in quanto modeste sono le esigenze nutritizie della mucosa.
Gli sperimentatori nipponici hanno provato a vedere se la mucosa rettale potesse “assorbire” ossigeno,
ottenendo un risultato – a mio modesto parere – molto limitato e poco riproducibile nell’uomo. Infatti, i
tessuti che troviamo a questo livello sono morfo-funzionalmente molto differenti da quelli che troviamo
nei polmoni, sviluppatisi in centinaia di milioni di anni di evoluzione di vita sulla Terra per espletare la
funzione dell’ematosi (lo scambio di ossigeno e anidride carbonica che avviene a livello degli alveoli
polmonari, dove il primo si sposta dall’aria al sangue e la seconda compie il percorso inverso).
Gli alveoli polmonari sono costituiti anch’essi da un unico strato di cellule epiteliali (come la mucosa rettale) ma le cellule sono molto basse (non “colonnari” ma piatte/pavimentose come delle “piastrelle”). Inoltre, queste cellule alveolari non si lasciano solo attraversare passivamente da ossigeno e anidride carbonica ma vi sono anche dei fenomeni attivi (vescicole che si spostano da un versante e l’altro della cellula, ossia dal versante “dell’aria” a quello “del sangue”), inesistenti a livello dell’epitelio rettale, che ne amplificano la funzione.
La superficie degli alveoli è ricoperta dal surfattante, una sostanza tensioattiva molto meno densa e meno spessa del muco presente a livello della mucosa rettale (muco che quindi rappresenta un ulteriore ostacolo per il passaggio dell’ossigeno dal lume rettale ai vasi della lamina propria della mucosa di quest’organo).
È vero che, se aumentando a dismisura la concentrazione di ossigeno nell’ampolla rettale, per banali leggi di diffusione legate alla fisica dei gas, un po’ di ossigeno riuscirà a superare la barriera costituita dal muco e dall’epitelio colonnare (barriera ben più spessa di quella presente a livello alveolare, quest’ultima costituita, come detto, dal surfattante e da un epitelio molto piatto), ma i capillari della lamina propria del retto non sono altrettanto numerosi e densi quanto quelli presenti nei sottili setti tra gli alveoli polmonari. Prova di tutto ciò ne è il fatto che, anche “raschiando” muco ed epitelio rettali, la ventilazione era inefficace (perché ciò che veniva determinato non era altro che una emorragia rettale) e le cavie comunque non sopravvivevano.
Mi sento pertanto di concludere che siamo ancora molto lontani da una sperimentazione di questa pratica nell’uomo. Bisognerebbe forse sviluppare, grazie alle biotecnologie e all’ingegneria biomedica, un sistema in grado di creare un ambiente rettale più consono all’assorbimento dell’ossigeno, ad esempio inducendo le cellule epiteliali rettali non solo a produrre un muco quanto più simile possibile al surfattante, per caratteristiche chimico-fisiche, ma anche a sviluppare dei sistemi di trasporto attivo delle molecole di ossigeno e anidride carbonica simili a quelli delle cellule alveolari; inoltre, bisognerebbe stimolare la proliferazione dei vasi della lamina propria rettale, per averne una concentrazione analoga a quella dei setti interalveolari. Bisognerebbe in pratica “alveolarizzare” il retto, inducendogli – in pochissimo tempo – delle trasformazioni morfologiche al momento inimmaginabili.
È vero che i confini della scienza esistono solo per essere varcati (al netto dei limiti imposti dalla bioetica), ma il confine che abbiamo appena tracciato non ci appare agevolmente varcabile con le attuali tecnologie a disposizione. Bisognerà in conclusione lavorare molto in questa direzione, oppure cercare altre strade, più agevoli.